Introdução a modelos atômicos
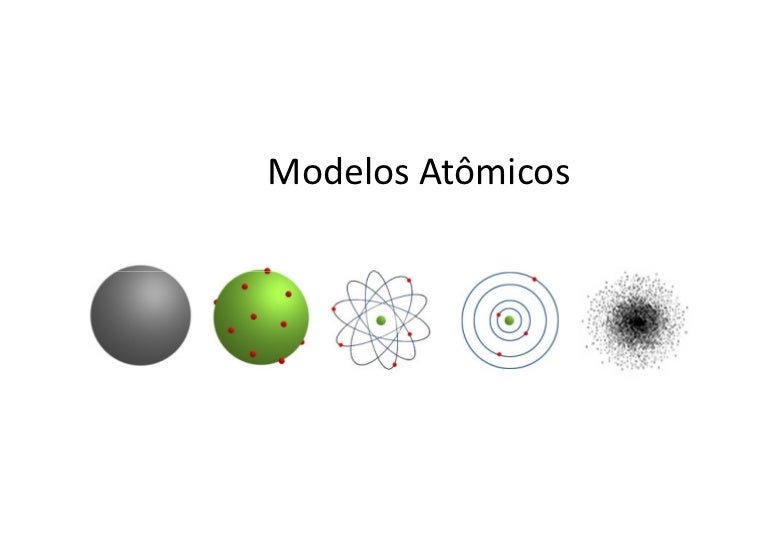
Olá outra vez dessa vez venho trazer um assunto muito relevante na área de astronomia: os modelos atômicos. Primeiramente precisamos esclarecer o significado de modelo, bem pense que você está fazendo uma escultura de um elefante, agora de isso para uma criança, ela associará a escultura a um elefante, no entanto não é um de verdade, é apenas um modelo de elefante. Dessa forma, podemos concluir que os modelos atômicos são apenas ideias de como podem ser o átomo, tendo em vista que não podemos enxergá-lo.
A primeira ideia que tivemos de algo parecido com um átomo veio da Grécia Antiga onde o filósofo Leucipo e seu discípulo Demócrito propuseram que o átomo seria o menor componente de toda a matéria existente, de fato, eles não estavam tão errados assim. O primeiro modelo científico foi criado por John Dalton, o qual era um meteorologista britânica, ele estudou por muitos anos gases rarefeitos e a composição atmosférica, a partir do seu conhecimento das leis ponderais chegou na sua definição de átomo – Segundo Dalton o átomo seria:
1 – Partículas extremamente pequenas
2 – Os átomos de um mesmo elemento são idênticos
3 – Um átomo não pode ser transformado
4 – Átomos de mais de um elemento se combinam
Depois disso vários experimentos realizados por químicos e físicos que estudavam o recém-descoberto fenômeno da radioatividade ajudaram a criação de novos modelos atômicos. Williaw Crookes foi um químico que assim como tantos outros voltou sua atenção para a radioatividade, seu experimento mais conhecido é chamado de Tubo de Crookes.
O experimento de Tubo de Crookes consiste em colocar um gás(fluorescente) em um tubo(pode ser uma garrafa), esse gás deveria estar a uma pressão muito baixa, logo em seguida é colocado um ânodo e um cátodo. O ânodo e o cátodo são basicamente o lado positivo e negativo de uma bateria, para mais fácil compreensão. Quando essa fonte de energia é ligada é possível observar uma linha se formando da direção do cátodo(negativo) para o ânodo(positivo). Essa linha foi chamada então de raios catódicos.
Depois de algum tempo um cientista chamado Joseph John Thomsom começou a estudar esses raios e tirou alguma conclusões interessantes:
1 – Os raios sempre saiam do cátodo para o ânodo e nunca o contrário
2 – Transferem momento, ou seja, esses tais raios possuem massa e podem movimentar o gás.
3 – Os raios catódicos se formavam independe mente do gás colocado.
Algum tempo depois de tirar essas conclusões ele pensou que poderia existir um motivo para o gás sempre sair do lado negativo e ser atraído em direção do lado positivo. Foi assim que surgiu o modelo atômico de Thomson, o qual tinha como objetivo esclarecer essas questões criadas pelo experimento de Crookes. No modelo de Thomson o átomo era representado como um pudim de passas, onde existira um núcleo sem carga ou com carga neutra e existiriam em volta desse núcleo elétrons com carga negativa.
Algum tempo depois dessa descoberta Ernest Rutherford, Geiger e Marsden realizaram a famosa experiência da folha de ouro, a qual consistia em bombardear uma fina folha de ouro com radiação. Note que o material escolhido para a experiência foi ouro, pois eles precisavam de um material resistente, uma folha de papel - por exemplo - não resistiria a radiação alfa, beta ou gama, além disso o ouro é um dos poucos metais que podemos laminar até virar uma folha. Após bombardear a folha com radiação foi notado que muitos raios (provenientes de um gás que estava na ampola) foram ricocheteados, o esperado seria que os raios passassem pela folha sem problemas. Após essa experiência Ernest Rutheford comentou que se sentiu como se tivesse atirado em uma folha de papel e o tiro voltado em sua cabeça.
Com as intrigantes questões causadas por essa experiência Rutherford criou o seu modelo, mais conhecido como modelo planetário do átomo, ou átomo clássico. O qual consistia de um núcleo central e os elétrons estariam em órbitas ao redor desse núcleo. Mais tarde com a descoberta dos raios anódicos, ou seja, a descoberta do próton novos modelos surgiram como o de Bohr e o modelo atômico atual.
No entanto, aqui começa a ficar um pouco mais complexo – portanto esse é assunto para um post separado, assim como o modelo atômico atual que será explicado em outra publicação.



Comentários
Postar um comentário